
Avaliação do potencial terapêutico dos psicadélicos em doenças neurológicas: não alucinogénicos vs alucinogénicos
28 de junho de 2024 • 6 minutos de leitura
- Pedro Mota
- Psicadélicos
Nos últimos anos, os psicadélicos como a psilocibina e o LSD têm ganho uma atenção significativa pelo seu potencial no tratamento de perturbações neuropsiquiátricas, como a perturbação obsessivo-compulsiva (POC), a depressão, a perturbação de stress pós-traumático (PSPT) e a dependência. Esta mudança de perspectiva está a conduzir a uma maior aceitação entre psicoterapeutas e psiquiatras, paralelamente ao uso clínico da escetamina. Simultaneamente, existe um interesse crescente na compreensão dos mecanismos pelos quais os psicadélicos e os seus análogos exercem os seus efeitos, com o objetivo de conceber novos produtos neurofarmacêuticos.
MECANISMOS DE ACÇÃO Os psicadélicos atuam principalmente através do recetor de serotonina 5-HT2A, que ativa as vias Gαq/11 e β-arrestina2 (Figura 1.). No entanto, ainda não é claro qual destas vias é mais crítica para os efeitos terapêuticos. Estudos recentes mostraram que os psicadélicos alucinogénios (por exemplo, psilocibina) e os psicadélicos não alucinogénios (por exemplo, Tabernanthalog ou TBG) podem activar diferencialmente estas vias. Esta activação diferencial pode levar a alterações nos estados da cromatina em potenciadores de genes envolvidos na organização de sinapses e plasticidade neuronal. Apesar destas descobertas, permanecem lacunas significativas na nossa compreensão dos mecanismos celulares e neuronais que ligam a plasticidade sináptica induzida por substâncias psicadélicas aos resultados comportamentais. Além disso, não se sabe se os psicadélicos não alucinogénios promovem a plasticidade através dos mesmos mecanismos.
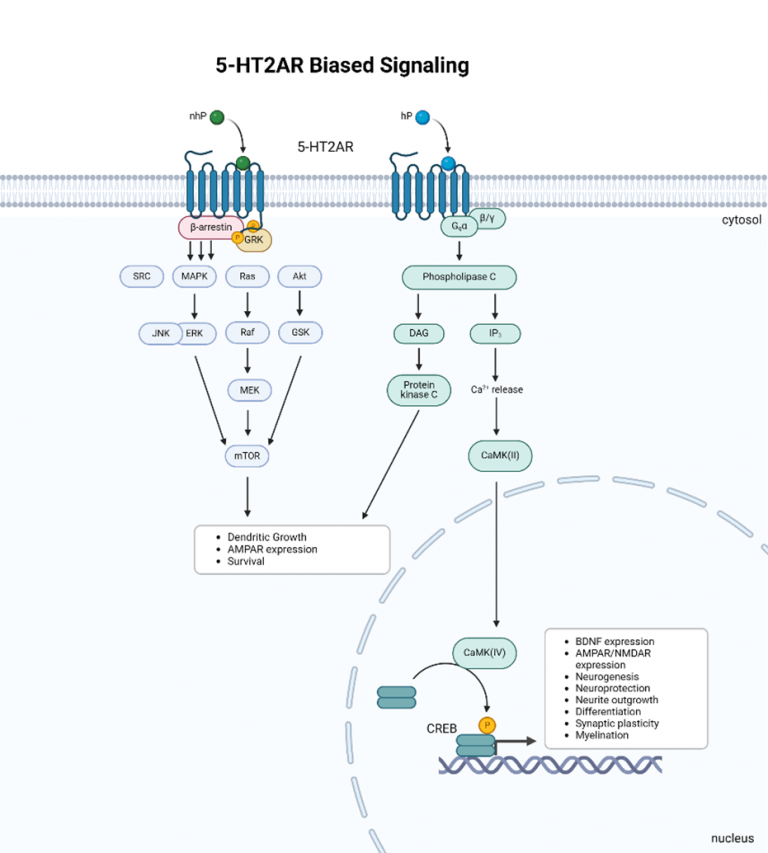
Figura 1. Sinalização enviesada de 5-HT2AR: dependente de Gq e dependente de beta-arrestina. nhP: psicadélicos não alucinogénios; hP: psicadélico alucinogénio.
PSICOPLASTÓGENOS: UMA NOVA CLASSE DE COMPOSTOS Os psicoplastógenos são substâncias capazes de induzir rapidamente a plasticidade neuronal estrutural e funcional, podendo modular as funções cognitivas. Estes compostos podem ajudar a resgatar a atrofia neuronal observada em muitas doenças neuropsiquiátricas e neurodegenerativas, modulando a expressão do fator neurotrófico, ativando os mecanismos de reparação neuronal e mediando as respostas imunitárias. O potencial terapêutico destes compostos tem sido cada vez mais reconhecido, enfatizando a necessidade de investigar os compostos naturais existentes antes de embarcar no longo processo de síntese de novos. Esta abordagem poderá aproveitar o conhecimento existente e reduzir os custos associados ao desenvolvimento de novas substâncias.
PSICADÉLICOS DIFERENCIADOS Os psicadélicos são uma família de substâncias psicoativas que induzem estados alterados de consciência, alterando profundamente os pensamentos, as emoções e as perceções. São distintos de outros compostos psicoativos, como os canabinóides (por exemplo, THC), os entactogénios (por exemplo, MDMA) e os dissociativos (por exemplo, cetamina). Apesar das regulamentações rigorosas e da ilegalidade em muitos países, existe a necessidade de desenvolver novas terapêuticas de base psicadélica com perfis farmacológicos otimizados para garantir a segurança e eficácia.
Os psicadélicos podem ser classificados quimicamente em três tipos principais: análogos da triptamina, derivados da ergolina e fenetilaminas.
ANÁLOGOS DA TRIPTAMINA Estes compostos partilham a espinha dorsal estrutural da serotonina. A psilocibina e o DMT são exemplos notáveis. A psilocibina, que se encontra nos “cogumelos mágicos”, é convertida no corpo na sua forma ativa, a psilocina, que produz efeitos que alteram a mente. O DMT induz experiências psicadélicas rápidas e intensas, mas tem uma ação de curta duração. É necessário equilibrar o potencial terapêutico com os fortes efeitos na sensopercepção para uso clínico.
DERIVADOS DE ERGOLINA O LSD é o principal exemplo desta classe, conhecida pelos seus potentes efeitos na sensopercepção. Estão em curso pesquisas para desenvolver derivados não alucinogénios que possam proporcionar benefícios terapêuticos sem as intensas experiências psicadélicas.
FENETILAMINAS A mescalina, derivada de certos cactos, é um composto chave nesta classe. Produz alterações na percepção visual e auditiva e tem sido estudada pelos seus potenciais efeitos terapêuticos.
AGONISTAS 5-HT2AR NÃO ALUCINOGÉNICOS É frequente acreditar-se que os efeitos terapêuticos dos psicadélicos estão associados às suas propriedades na sensopercepção. No entanto, a evidência pré-clínica sugere que estes efeitos podem ser separados. Isto levanta uma questão importante: como podemos preservar os benefícios terapêuticos dos psicadélicos e, ao mesmo tempo, minimizar ou eliminar os efeitos alucinogénios? Foi identificado um número limitado de agonistas 5-HT2A não alucinogénios. Por exemplo, o 6-F-DET, um análogo da triptamina, não tem efeitos alucinogénios, mas também tem uma fraca atividade funcional. Os derivados da ergolina, como o 2-Br-LSD e a lisurida, demonstraram potencial no tratamento da depressão e de outras perturbações psiquiátricas em estudos com animais, embora a lisurida tenha induzido alucinações em alguns doentes com doença de Parkinson.
Os derivados do isoDMT, introduzidos na década de 80, representam outro grupo de agonistas 5-HT2A não alucinogénios. Compostos como o isoDMT e o 5-OMe-isoDMT foram identificados como não alucinogénios através de testes de discriminação de drogas. Estudos recentes do grupo Olson reportaram uma série de compostos isoDMT que promovem o crescimento neuronal e têm efeitos antidepressivos significativos em modelos de ratinhos, apresentando um interesse significativo como psicoplastógenos para aplicações clínicas 8. Um destes compostos, o AAZ-A-154, mostrou-se promissor como um psicoplastógeno não alucinogénio. Verificou-se que outro composto, o TBG, um análogo simplificado da ibogaína, aumenta a arborização dendrítica e a densidade da coluna vertebral nos neurónios corticais de ratos.
DIREÇÕES FUTURAS E APLICAÇÕES CLÍNICAS O potencial para redirecionar os psicadélicos para o tratamento não só de distúrbios cognitivos, mas também de condições neurológicas caracterizadas por atrofia neuronal está a crescer. No entanto, ainda são necessárias pesquisas substanciais para elucidar como estes compostos estimulam os mecanismos neuroplásticos. É crucial determinar os estádios de desenvolvimento em que o tratamento é mais benéfico e compreender como estes compostos afetam as redes neuronais em diferentes escalas.
Do ponto de vista da química medicinal, existe uma necessidade urgente de desenvolver novas entidades químicas com perfis farmacológicos otimizados para criar terapêuticas de base psicadélica mais eficazes e seguras. Isto inclui o apoio à investigação sobre agonistas dos recetores 5-HT2A para utilização em várias perturbações, começando pelos antidepressivos. Sabe-se que as perturbações na sinalização do recetor 5-HT2A estão implicadas em perturbações mentais, como a esquizofrenia, a depressão, a ansiedade e a dependência.
Estão a ser desenvolvidas técnicas avançadas para investigar minuciosamente as propriedades alucinogénias dos psicadélicos. Estes incluem novos recetores recombinantes e ensaios funcionais otimizados que ajudam a compreender os mecanismos moleculares subjacentes aos efeitos terapêuticos dos psicadélicos. À medida que estes compostos avançam para ensaios clínicos, é essencial desenvolver e utilizar modelos pré-clínicos apropriados que possam medir com precisão os seus comportamentos alucinogénios. Embora traduzir as descobertas de roedores para humanos seja um desafio, ensaios comportamentais como o Head-Twitch Response (HTR) foram desenvolvidos para distinguir entre psicadélicos alucinogénios e não alucinogénios in vivo.
CONCLUSÃO Existe um espaço crescente para o uso terapêutico de compostos psicadélicos, que podem potencialmente ser aplicados a perturbações cognitivas e neurológicas caracterizados por atrofia neuronal. No entanto, é ainda necessária uma quantidade considerável de investigação para compreender completamente como estes compostos estimulam a neuroplasticidade e determinar as fases mais eficazes para o tratamento. Este conhecimento ajudará no desenvolvimento de novas terapias que possam manipular eficazmente as redes neuronais e proporcionar benefícios significativos para uma série de condições cerebrais.
Artigo original de Guilherme Gabriel no blogue da OPEN Foundation. Tradução livre por Pedro Mota

Pedro Mota
Mais posts

- Pedro Mota
- MDMA
- Psiquiatria
Follow-up de longo prazo de Ensaio Clínico de fase 3 da MAPS sobre Terapia Assistida por MDMA para PTSD
A MAPS Public Benefit Corporation (MAPS PBC), uma subsidiária da Multidisciplinary Association for Psychedelic Studies (MAPS), anunciou os r...

- Pedro Mota
- Psicadélicos
Número Especial do Journal of American Psychiatry centra-se nos Psicadélicos
À medida que o corpo de evidência sobre o potencial promissor das medicações psicadélicas em Psiquiatria cresce, permanecem muitas questões...
